SAVIについて
WASAVIsでは、現在「SAVI(Strut Adjusted Volume Implant)を用いた乳房温存術後
小線源治療の治療効果に関する多施設共同観察研究」を行っております。
ご興味のある先生は、是非WASAVIs事務局へご連絡ください。
東京医科歯科大学医学部附属病院放射線治療科 吉村亮一
E-mail : info@wasavis.jp
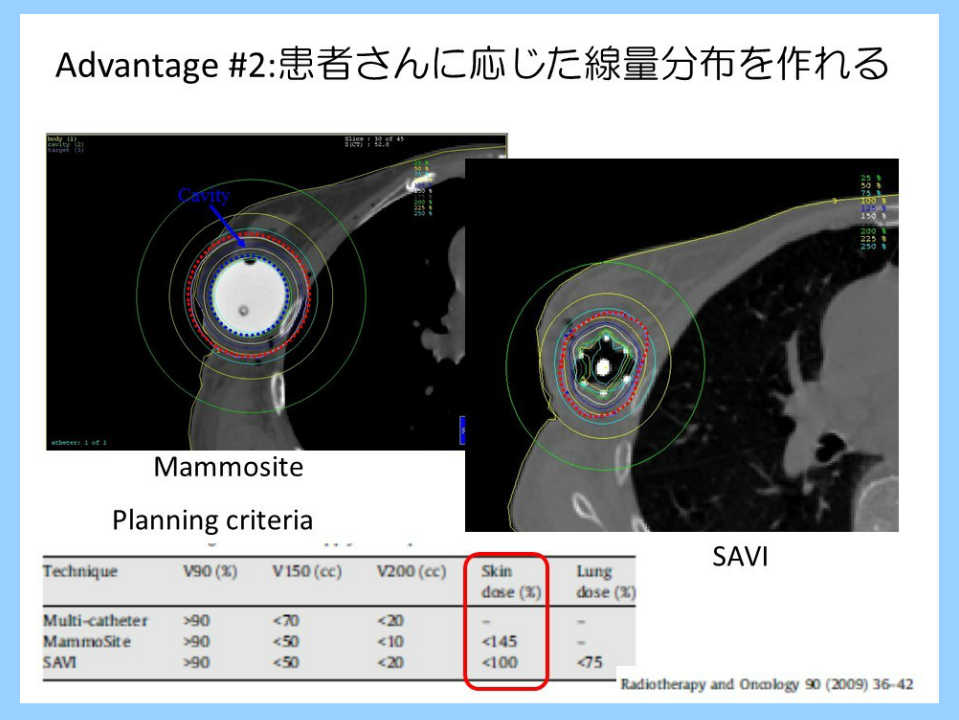
SAVI(Strut Adjusted Volume Implant)を用いた乳房温存術後
小線源治療の治療効果に関する多施設共同観察研究(UMIN ID: UMIN000021237)
研究代表者:伊丹 純
国立がん研究センター中央病院 放射線治療科
研究事務局:吉村 亮一
東京医科歯科大学医歯学総合研究科腫瘍放射線治療学分野
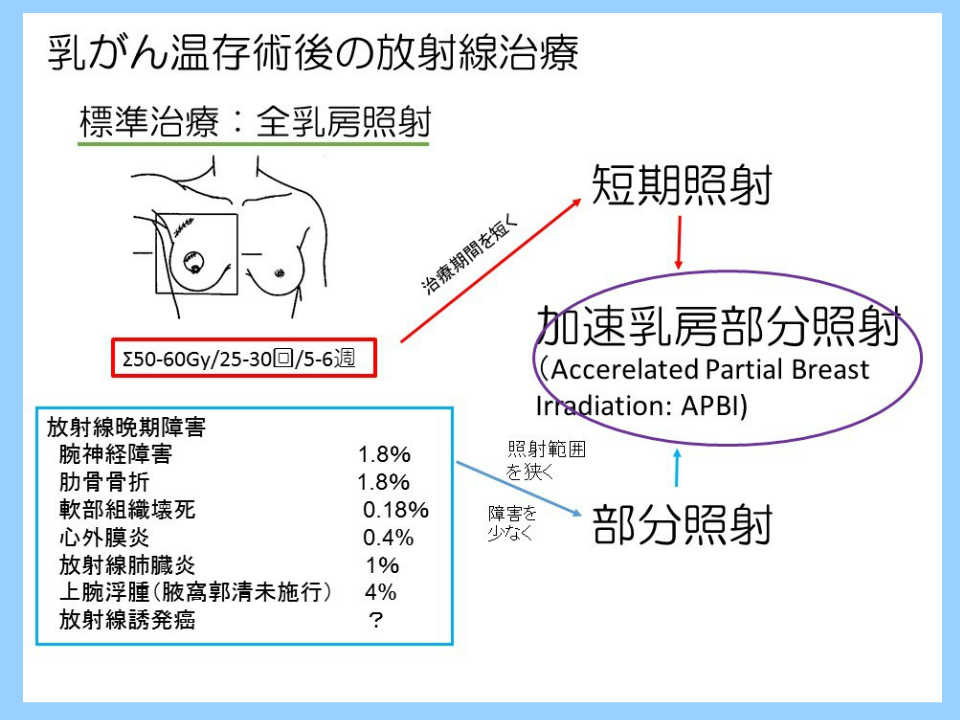
0. 概要
0.1. シェーマ

0.2. 目的
本研究では、早期乳癌を対象として部分切除後にSAVI法を用いた小線源治療を行う乳房温
存療法の有効性を多施設で評価する。
Primary endpoint: 局所制御割合
Secondary endpoints: 無病生存割合、全生存割合、有害事象、整容性評価、放射線量
評価
0.3. 対象
- 1) 一次登録
- ① 臨床的に腫瘍径3cm以下の乳癌で乳房温存療法が予定されている
- ② 臨床的にリンパ節転移および遠隔転移を認めない
- ③ 臨床的に原発巣がunifocalかつ unicentric(異なる4分割領域にも、4cm以上離れた部位にも独立した 乳癌病巣がない)である
- ④ 生検の結果、病理組織学的に乳管癌(浸潤性・非浸潤性)あるいは粘液癌、髄様癌、管状癌、小葉癌 (浸潤性・非浸潤性)である
- ⑤ 乳癌の既往がなく、同時対側乳癌もない
- ⑥ 治療予定の乳癌に対して、過去に放射線療法または化学療法の既往がない
- ⑦ 40歳以上で説明同意文書を十分理解できる女性
- ⑧ Performance Status (ECOG)が0~1である。
- ⑨ 患者本人が乳癌の告知を受けており、さらに本研究に関し文書による同意が得られている
- 2) 最終登録
- ① 一次登録がされている
- ② 乳房部分切除術が施行され切除腔が形成されている
- ③ 原発巣が病理学的に腫瘍径3cm以下である
- ④ 最終病理診断で乳管癌(浸潤性・非浸潤性)あるいは粘液癌、髄様癌、管状癌、小葉癌
- (浸潤性・非浸潤性)である
- ⑤ 最終病理診断で広範囲乳管内進展を認めない
- ⑥ 最終病理診断でリンパ管侵襲および静脈侵襲を認めない
- ⑦ 標本の染色された断端が病理組織学的に陽性ではない(浸潤癌または非浸潤癌が染色された切除断端に 露出して存在する場合を断端陽性とする)
- ⑧ センチネルリンパ節生検あるいは腋窩郭清によってリンパ節転移がないことが確認されている。ただ し、非浸潤性乳管癌の場合はセンチネルリンパ節生検の省略も可
- ⑨ 当該乳癌に対して内分泌療法は随時行って良いが、化学療法を行う場合はSAVIアプリケーター抜去後2 週間以上経てから開始する
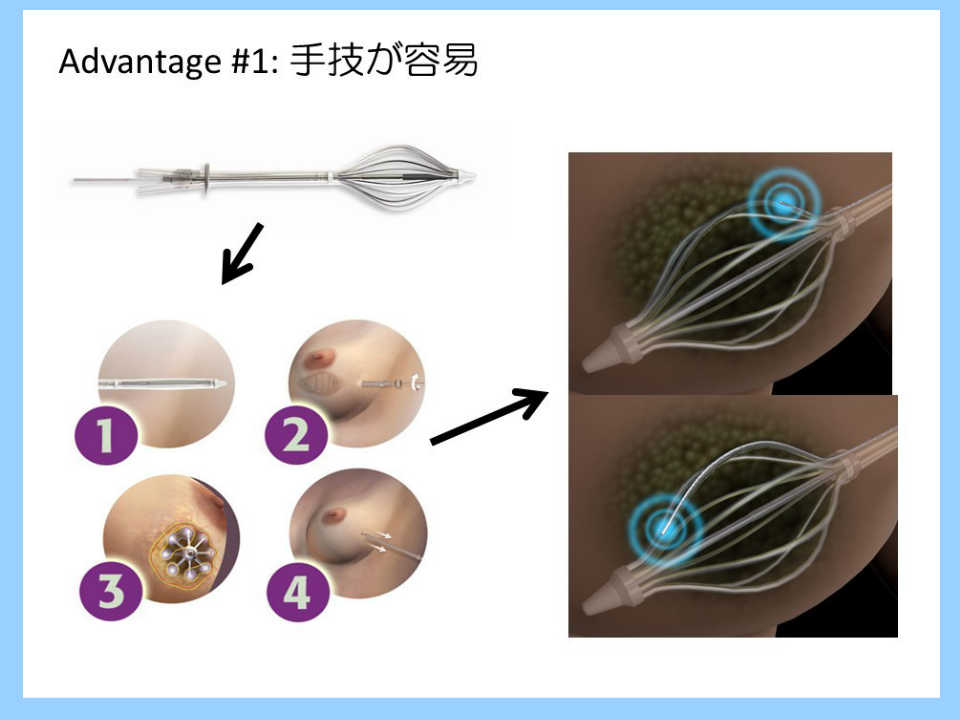
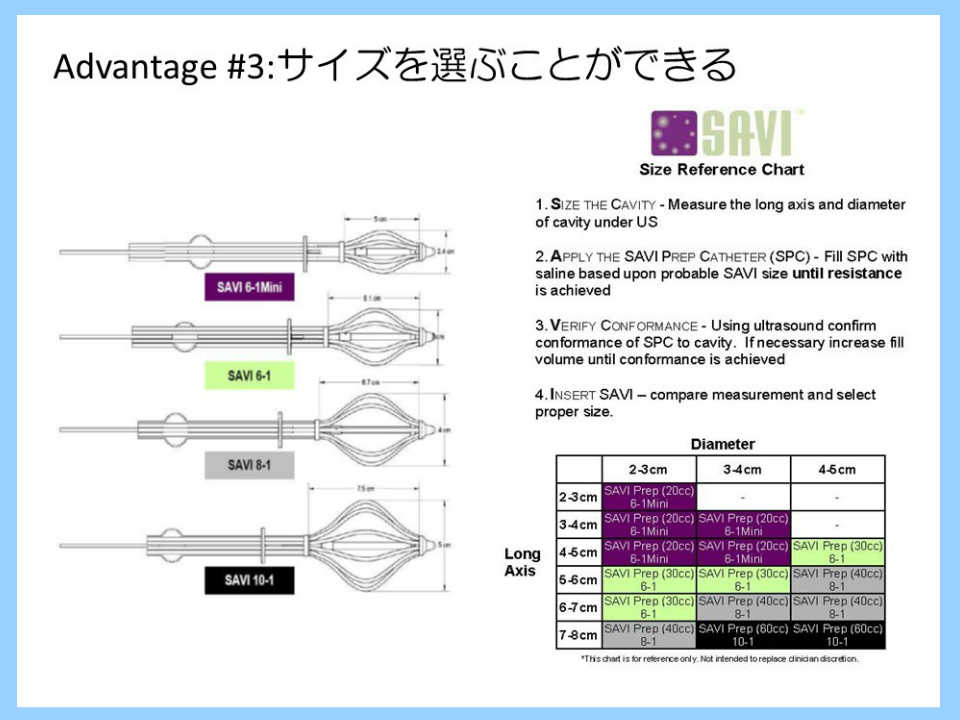
0.4. 治療
乳房部分切除後、永久標本での断端陰性等が確認され最終登録を行った後、SAVIアプリケ
ーターを術腔に挿入しRemote After Loading System (RALS)による高線量率小線源治療
を行う。本研究では術中にスペーサーを留置し、最終病理結果確認後SAVIアプリケーター
に入れ換える方法(術中スペーサー留置法)と、手術では閉創し最終病理結果確認後、
SAVIアプリケーターを経皮的に挿入する方法のいずれも許容する。
処方線量は1回3.4Gy、1日2回(6時間以上の間隔を空ける)、総線量34Gyとする。
最後の照射が終了したのちにアプリケーターを抜去する。
0.5. 予定登録数と研究期間
1.予定登録症例数: 82例(最終登録症例)
2.登録期間: 5年間、追跡調査期間 5年間
研究期間は計10年間とする。
0.6. 研究実施機関
国立がん研究センター中央病院、
東京医科歯科大学医学部附属病院、
昭和大学病院、
福山医療センター、
関西医科大学総合医療センター、
神奈川県立がんセンター、
鹿児島市立病院、
岡山大学病院、
徳島大学病院、
徳島赤十字病院
乳がん小線源治療用のアプリケーターSAVI(サヴィ)の動画
〈2022年6月1日 SAVIを用いた小線源治療 アップデート版〉
小線源治療 3回照射 のことが語られています。
〈2018年9月30日 SAVIを用いた小線源治療を受けられて〉
SAVI治療を受けられた感想が語られています。